Partículas Elementales y Antimateria
|
Actividad de Aprendizaje: |
Tabula las principales Partículas
Elementales y sus propiedades. |
Las partículas que usaremos para explicar
estos fenómenos relacionados con
|
Partícula |
Símbolo |
Masa (u. m. a.) |
Carga |
|
Protón |
p, 1H1 |
1.00760 |
+e |
|
Neutrón |
n, 0n1 |
1.00898 |
0 |
|
Electrón |
-1e0 , -1b0 |
0.0005488 |
-e |
|
Positrón |
+1e0 , +1b0 |
0.0005488 |
+e |
El núcleo de un átomo está formado por dos
partículas con excepción del átomo de hidrógeno que solo tiene un protón, la
otra partícula es el neutrón.
Al número de protones que tiene el núcleo
de un átomo se le denomina número
atómico.
A la suma de protones más neutrones más
protones que tiene el núcleo de un átomo le llamamos masa o peso atómico del
átomo.
Los átomos tienen la misma cantidad de
protones en el núcleo que de electrones girando alrededor de éste, por esto se
considera cero la carga de cualquier elemento.
La cantidad de neutrones en el núcleo es
igual o mayor a la cantidad de protones. Cuando dos átomos tienen el mismo
número atómico y diferente peso, los átomos son isótopos, por ejemplo, el oxígeno tiene un número atómico 8 y sus
isótopos tienen masas de 16, 17 y 18, aquí simbolizamos a estos isótopos como
sigue: 8 O 16 , 8 O 17
, 8 O 18 ; el número 16 significa 8 protones y 8
neutrones; el número 17 significa 8 protones y 9 neutrones; el número 18
significa 8 protones y 10 neutrones.
Unidad de Masa Atómica (u. m. a.)
La unidad de masa atómica es igual a un
doceavo de la masa de la forma más abundante de la masa del carbono.
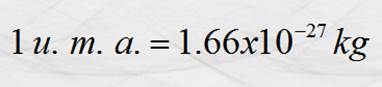
Energía de Enlace
Los núcleos de los átomos están unidos por
cuatro fuerzas denominadas : Fuerza
gravitacional, que es la de menor intensidad; Fuerza débil, mayor que la anterior; Fuerza electromagnética debida al movimiento relativo de las
cargas, mayor que la anterior; y Fuerza
Fuerte, más grande que la electromagnética, solo para distancias pequeñas.
La fuerza fuerte es la que mantiene unidos
a los protones y neutrones en espacios tan pequeños como 10-15 m
; a esta distancia es cuando es más efectiva
esta fuerza; la fuerza fuerte se reduce cuando los núcleos crecen y se hace
sentir más la fuerza electromagnética.
La masa del núcleo de un átomo es diferente a la suma de las masas de sus
componentes. Si
sumamos la masa de dos protones más la masa de dos neutrones, obtenemos la suma
de los componentes del núcleo de un átomo de helio; y si comparamos esta masa
con la masa del núcleo de un átomo de helio encontraremos que la suma de los
componentes es ligeramente mayor que la masa del núcleo. La diferencia de estas
masas (la de las componentes menos la del núcleo), es igual a la de la energía
equivalente liberada cuando con los componentes formaron el núcleo. El
equivalente en energía de la diferencia de masas se calcula con el modelo de la
energía cinética de Einstein, E = m C2:
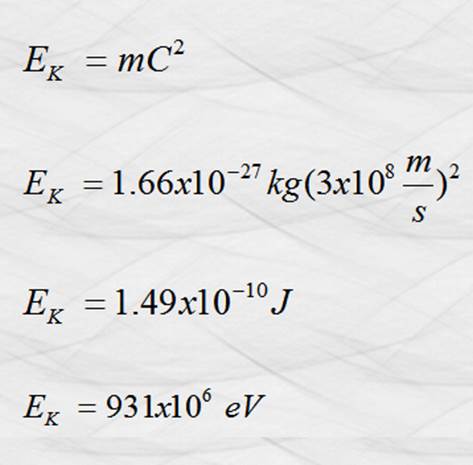
Un eV
(electrón Volt) es unidad de energía
usada en estos análisis y es igual a la energía necesaria para un electrón a lo
largo de una diferencia de potencial de un volt.
A la energía equivalente de la diferencia
de masa citada se le denomina energía de
enlace y corresponde con la energía que une las partículas del núcleo de un
átomo.
Antipartícula y Antimateria
Se ha descubierto que cada partícula elemental
de las mencionadas y de otras que aparecen espontáneamente durante los procesos
nucleares tienen su antipartícula, es decir éstas son partículas semejante a
cualquiera de las mencionadas pero con una característica esencial contraria,
por ejemplo, se ha descubierto positrones, partículas semejantes a los
electrones pero con carga positiva; otra de las partículas descubiertas son los
antiprotones; antineutrones ; se ha llegado a pensar en antiátomos,
incluso antimateria que forme un antiuniverso. En
particular, el fotón no tiene, o no se ha encontrado un antifotón.
Se dice que cuando dos antipartículas
chocan, como un electrón y un positrón,
desaparece la materia y en su lugar aparece otra forma de energía como son los
fotones, con igual impulso lineal y conservándose la energía